Information » Wirkprinzip
Wirkprinzip
EDTA-CHELAT-THERAPIE
Chemisches und pharmakologisches Wirkprinzip von EDTA
Die Wurzeln der Chelat-Therapie sind über 100 Jahre alt. Doch wie in vielen anderen Fällen auch hat der Anfang der Geschichte noch überhaupt nichts mit der Chelat-Therapie, so wie wir sie heute kennen, zu tun.
Zunächst war da erst einmal die Entdeckung einer biochemischen Verbindung 1893 in einem Schweizer Labor, deren Bedeutung man nicht erkannte.
Wer konnte damals schon richtig einschätzen, dass eine chemische Verbindung, die man später als Chelatbildner bezeichnete.Schwermetalle, Metalle und andere Schadstoff binden kann, die normalerweise nicht wasserlöslich sind und die man auf diese Weise schadlos aus vielen Substanzen entfernen kann.
Später dann, fand man in der Zitronensäure eine Substanz, die "unerwünschte Bestandteile" aus den Textilien entfernte, ein wichtiger Produktionsschritt in der Textilindustrie!
Durch die wirtschaftliche und politische Isolierung der Kriegszeit suchte man in Deutschland nach einem Ersatzstoff für die Zitronensäure. Man fand diesen in einer Substanz, die man mit Ethylen-Diamin-Tetraazetat (EDTA) bezeichnete. Dieses Produkt war zum Beispiel in der Lage, Kalkflecken aus Textilien zu entfernen.
Recht bald erkannte man aber,dass dieser Stoff auch ein idealer Zusatz von Wasch- und Reinigungsmitteln ist und dass man auch in der Pharmaindustrie Mineralien und bestimmte Medikamente an Chelatkomplexe binden kann, damit sie besser in den Körper aufgenommen werden.
All das geriet nach Ende des Zweiten Weltkrieges aber wieder in Vergessenheit. Es waren dann die Amerikaner, die 1945 die Patente übernahmen mit der Absicht, EDTA auch bei radioaktiven Verseuchungen einzusetzen, um die strahlungsaktiven Isotope aus dem Körper zu entfernen.
Die Bedeutung des Chelatbildners EDTA für die Medizin wurde erstmals bekannt, als Arbeiter einer Akkumulatorenfabrik, die an einer Bleivergiftung litten, mit dieser Substanz behandelt wurden und sich schnell von ihrer toxischen Belastung erholten.
Hier setzt auch mein Kontakt mit Chelat an, da ich in meiner wissenschaftlich aktiven Zeit in Heidelberg mit Flavonoiden und Anthocyanen gearbeitet habe. Flavonoide sind phantastische Komplexbildner und zum Teil auch Chelatbildner, die sich zur Entgiftung nicht nur von Schwermetallen eignen.
Doch wo liegt der Unterschied?
Das Wort Chelat leitet sich vom griechischen Wort Chele = Krebsschere ab und wurde 1920 durch Morgan und Drew als Sammelbezeichnung für solche cyclischen Verbindungen eingeführt, bei denen Metalle, Gruppierungen mit einsamen Elektronenpaaren oder mit Elektronenlücken und Wasserstoff an der Ringbildung beteiligt sind.
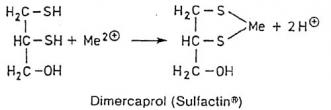
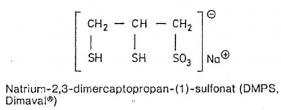
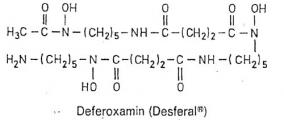
| Mg: 292,2 | C10H16N2O8 |
| weißes, kristallines Pulver; Schmp.220°C | |
| Löslichkeit: | sehr schwer löslich in H2O |
| gut löslich Alkalihydroxidlösung |
Durch Ansäuren auf Ph 5 entsteht das Dinatriumsalz der Edetinsäure, ein weißes kristalline Pulver, Mg 372,2, das nun leicht in Wasser löslich ist.
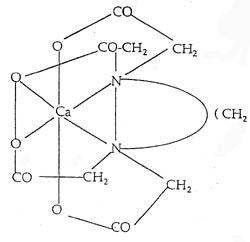
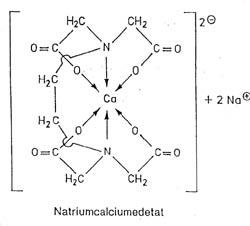
EDTA hat 6 frei Elektronenpaare, die sie dem Metall-Kation anbieten kann. Zwei der Aminogruppen und vier der Sauerstoffatome der Säuregruppen. Diese sechs Atome werden auch als die Zähne des EDTA-Moleküls bezeichnet, die z.B. das Ca (siehe Abbildung) binden.
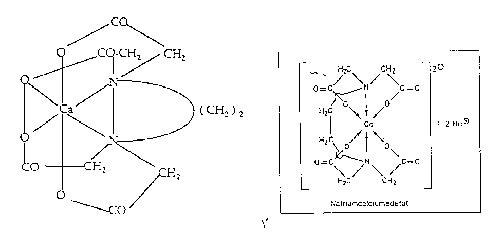 Die Strukturformel zeigt, dass das Metall in einen heterocyclischen Ring eingebunden ist, dabei wird die Reaktionsfähigkeit des Kations aufgehoben und verliert seine Eigenschaft. Für die Bildung von EDTA- Komplexen sind ein paar wichtige Faktoren zu beachten.
Die Strukturformel zeigt, dass das Metall in einen heterocyclischen Ring eingebunden ist, dabei wird die Reaktionsfähigkeit des Kations aufgehoben und verliert seine Eigenschaft. Für die Bildung von EDTA- Komplexen sind ein paar wichtige Faktoren zu beachten.
| 1. | PH-Wert. Mit ansteigendem PH wird das Chelat stabiler und verliert weniger leich sein Metallion. In vitro sind die stabilsten Chelate im basischen, in vivo haben wir natürlich eine strenge Abpufferung des Blut-PH. |
| 2. | Bindungsstärke: Die Affinität verschiedener Metallionen zu einem Chelatagens ist unterschiedlich. Bei konkurrierenden Metallionen wird das Ion mit der größeren Affinität komplexieren. Man kann diese auch mathematisch mit der Stabilitätskonstante Ks ausdrücken. Je größer diese Konstante ist, desto größer ist die Bereitschaft zu komplexieren und desto stabiler ist das Chelat. Die Werte werden logarithmisch angegeben, als LogK. |
| etall-Kation | Log K |
| Fe+++ | 25.1 |
| Hg++ | 21.8 |
| Cu++ | 18.8 |
| Pb++ | 18.5 |
| Ni++ | 18.0 |
| Zn++ | 16.5 |
| Cd++ | 16.5 |
| Co++ | 16.3 |
| A1+++ | 16.1 |
| Fe++ | 14.3 |
| Mn++ | 13.7 |
| Ca++ | 10.7 |
| Mg++ | 8. |
Wie man aus der Tabelle leicht ersehen kann, haben die Schwermetalle wie Eisen, Kupfer und Quecksilber eine sehr hohe Affinität, während die Erdalkalimetalle wie Magnesium und Calcium geringeren und die monovalenten Alkalimetalle wie Kalium und Natrium die geringste Affinität besitzen und damit auch die kleinste Stabilitätskonstante.
Die in der Praxis interessanten Metallionen sind also di-oder trivalent.
| 3. | Konzentration: Die relative Konzentration spielt auch eine gewisse Rolle, so können Metalle niederer Affinität in großer Konzentration Metalle mit stärkerer Affinität verdrängen. So ist z.B. Calcium in vivo stark chelatiert, obwohl es in der Liste weit unten steht, da es im Plasma doch in einer relativ hohen Konzentration vorkommt! |
| 4. | Interaktionen in vivo: Die Stabilitätskonstante wurden in vitro ermittelt. In vivo gibt es allerdings noch eine ganze Reihe endogener Liganden, die mit EDTA um das Metallion konkurrieren können, so sind die aktiven Metallionen an Protein, Enzyme oder Transportprotein wie z.B. das Transferrin gebunden. Das heißt, die so gebundenen Metalle werden kaum aus ihrer physiologischen Verbindung gerissen, es geht viel mehr um ungebundene, freie, meist toxische Metallionen, die in kleinen Mengen vorkommen |
Quintessenz der Bindungsaffinität:
Sobald EDTA in die Blutbahn gerät lässt es das Magnesium frei, bindet das Calcium, lässt auch dieses frei, wenn sich ein Metallion mit höherer Affinität findet ( meist toxischer) usw., mit dem toxischen Metall höhster Affinität verlässt es über die Niere den Körper.
Wenn wir von EDTA-Dinatriumsalz sprechen, müsste man korrekterweise auch die beiden Wasserstoffe der vier Säurereste benennen, die nicht mit Na+ neutralisiert sind und deshalb auch noch frei sind für eine weitere Neutralisation. In der Praxis wird das mit einer berechneten Menge Magnesium getan. Wenn also eine Infusion von EDTA ins Blut gelangt, so wird bei einer relativ hohen Ca-Konzentration, das Mg sofort als Mg-Ion freigesetzt.
Es muß nochmals betont werden, das nur Metalle die frei in ionisierter Form oder in nur schwacher Bindung vorliegen, Chelate bilden können, während Metalle, die in fester chemischer Bindung mit Phosphaten oder Silicaten, wie z.B. in unserem Skelett, nicht zugänglich sind. Um dennoch toxische Schwermetalle komplett eliminieren zu können, müssen die Infusionen öfter wiederholt werden und es muss genügend. Zeit gegeben werden, bis sich ein Gleichgewicht eingestellt hat zwischen gebundenem und freiem Schwermetallion im Blut.
Pharmakologie
Die Chelattherapie mit intravenöser Gabe von Ethylendiamintetraessigsäure (EDTA) wird seit etwa 30 Jahren von einer ständig zunehmenden Zahl von Ärzten angewandt. Es ist inzwischen bekannt, dass beobachtete Nierenschäden oder andere unerwünschte Effekte der Chelattherapie auf eine zu rasche Infusion (unter 2Std.) oder Überdosis (50mg/kg Körpergewicht überschreitende Menge) bei gleichzeitig vorgeschädigter Niere, bzw. schweren Bleivergiftungen, zurückzuführen sind.
Wegen der relativ großen Menge freien ionisierten Calcium im Blut kann eine schnelle i. V.-Infusion von EDTA zu einer hypocalcämischen Tetanie führen. Eine langsame Infusion etwa I5mg/Min, (ca.25-40Tropfen) führt generell nur zu einer geringen Abnahme von freien Serumkalzium und vermeidet die Gefahr einer Tetanie.
Wenn die EDTA-Lösung langsam über längere Zeit infundiert wird, geht das Calcium aus anderen Zelldepots wie Zell- und Gefäßwänden sowie Knochen in die Lösung und wird im Urin ausgeschieden.
Eine langsame Reduktion von Semmkalzium stimuliert die Sekretion von Parathormon
und es bleibt dabei das Serum-Calcium unverändert. Theoretisch werden bei einer i.V.-Infüsion von 3g EDTA 324 mg. Calcium ausgeschieden, das ist etwa die doppelte Menge einer physiologischen täglichen Ausscheidung.
Ein weiterer wichtiger Aspekt von EDTA-Infusion betrifft den Knochenmetabolismus. Wie erwähnt verursacht die Reduktion von Serumcalcium eine schnelle Ausscheidung von Parathormon um den Ca-Verlust auszugleichen.
Bei einem primären Hyperparathyreoidismus sind die Ruhe-PTH-Spiegel erhöht und die EDTA-Therapie führt zu einer überschießenden Reaktion. Beim Hypoparathyreoidismus sind die Ruhe-PTH-Spiegel innerhalb der Norm, aber die EDTA-Therapie führt zu keiner oder doch nur schwachen Reaktion. Bei einem latenten Hypoparathyreoidismus bleiben die Calciumspiegel 12 Stunden nach einer EDTA-Stimulierung gesenkt.
Durch die kurzzeitige, rhythmische Zunahme von Parathormon bei der EDTA-Therapie kommt es nach einer 3-4 wöchigen osteoklastischen Phase zu einer anschließenden 2-3 monatigen osteoblastischen Phase, in welcher es zu verstärkter Knochenneubildung kommt. Man spricht sogar von einer signifikanten Verbesserung der Knochendichte 2-3%. Wenn von vorneherein das Calciumsalz von EDTA verwendet wird, verändert sich das Calcium Gleichgewicht im Serum nicht.
Das Dinatrium-EDTA-Molekül wird nicht metabolisiert und auch nicht resorbiert. Nach intravenöser Infusion der EDTA Lösung bildet sich aus Na2-EDTA CaNa2-EDTA, das rasch im Urin ausgeschieden wird. Etwa 50% verlassen den Körper in einer Stunde und über 95% innerhalb von 24 Stunden. Mit radioaktiv markierter Substanz wurde festgestellt, dass nach 4S Stunden nur noch 0,5% im Körper vorhanden sind. Es wird vermutet, dass dieser nur langsam ausgeschiedene Reste an Eisen gebunden ist. Weniger als 0,1% erscheinen als CO2 in der Atemluft. Die rasche Ausscheidung durch die Nieren ist darauf zurückzuführen, dass die Substanz sowohl im Glomerulum filtriert als auch irn Tubulus sezerniert wird.
Vorsicht ist geboten bei Patienten mit eingeschränkter Nierenfunktion, die Ausscheidung von EDTA kann wesentlich verzögert sein.
EDTA ist eine relativ untoxische Substanz, da sie nicht metabolisiert und sehr schnell ausgeschieden wird. Die Verabfolgung zu hoher Dosen in zu kurzer Zeit kann Nierenschädigungen hervorrufen, durch Freisetzung von Schwermetallen in den Nierentubuli.
Renale Irritationen mit leichtem Anstieg der Harnstoff- und Kreatininwerte sind in der Regel reversibel und verschwinden nach Absetzen der Therapie in wenigen Tagen.
Allergien und anaphylaktische Reahionen auf EDTA treten äußerst selten auf. Dies kann jedoch der Fall sein, falls den EDTA-Infusionen Zusätze, wie Vitamine des B-Kompiexes, Procain etc., beigemischt werden.
Häufig wird nach Infusion von EDTA-Lösung eine Senkung des diastolischen und systolischen Blutdruckes um 5 bis 20 mm Hg beobachtet.
Ich möchte noch mal betonen, was geschieht, wenn wir EDTA infundieren; EDTA bindet Metalle, dass ist alles. Doch dieses Effekt hat eine Kaskade von Folge Wirkungen. Die Entfernung von toxischen Mineralien wie Blei, Arsen, Nickel und Aluminium hat eine große Bedeutung für unser Enzym-System, Immunsystem, Mitochondrien und den frühen Zelltod.
Neuere Entdeckungen auf dem Gebiet der Pathologie der freien Radikale stellen eine umfassende wissenschaftliche Grundlage dar, um die günstigen Auswirkungen der EDTA-Chelat-Therapie zu erklären.
Die EDTA kann die Produktion der freien Radikale millionenfach reduzieren.
Der fortschreitende Prozess der schädlichen Lipidoxidation durch die freien Radikale ann durch Dekorporation von zuweilen in Spurenmengen vorhandenen Schwermetallen und des dislozierten Eisens und Kupfers mittels EDTA bis um das Millionenfache gehemmt werden.
In Gegenwart von EDTA können die Metall-Ionen die Entstehung der freien Radikale nicht katalytisch beschleunigen. Spuren von ungebundenen Metall-Ionen sind für unkontrollierte Proliferation der freien Radikale im Gewebe erforderlich. EDTA bindet die ionisierten Metallkatalysatoren, macht sie dadurch chemisch inert und entfernt sie aus dem Körper.
Die Chelat-Therapie reaktiviert Enzyme durch Entfernung de toxischen Schwermetalle. Der Bleigehalt in Knochen hat sich beim Menschen seit Beginn der industriellen Revolution mehr als verfünfhundertfacht. Die Fähigkeit Mineralien aus Leber und Niere zu beseitigen entlastet diese Organe wesentlich.
Die Entfernung von sog. essentiellen Mineralien wie Eisen, Kupfer, Zink, Mangan und Kalzium sofern sie ungebunden ionisch vorkommen, vermindert die Aktivität der freien adikale und fuhrt zu einer Veränderung der Zellfunktion, Stabilisierung der ellmembran und Unversehrtheit der Blutplättchen.
Weitere günstige Auswirkungen der Chelat-Therapie kommen zustande durch Entkoppelung der Disulfidbrücken und metallischen Quervernetzungen, durch Normalisierung des Calciumstoffwechsels, durch Reaktivation von Enzymen, die durch Blei oder andere toxische Metalle inhibiert wurden, und durch Wiederherstellung normaler Prostacyclin-Produktion in der Gefäßwand. Die Bedeutung und Interpretatien all dieser Effekte wird an anderer Stelle diskutiert.
Bei oraler Verabreichung von EDTA werden nur etwa 5% vom Gastrointestinaltrakt resorbiert, der Rest wird über den Stuhl ausgeschieden. Oral verabreichtes EDTA kann sogar im Darm Spurenelemente binden und deren Resorption verhindern. Man kann sich sogar ein Einschleusen von toxischen Mineralien vorstellen; Aus diesen Gründen kommt die orale Verabreichung in praxi nicht in Frage!
Kleine Mengen von EDTA können auch über die Haut resorbiert werden. Man kann auch klein Konzentrationen von EDTA in der Spinalflüssigkeit nachweissen nach einer Infusionstherapie. Intramuskuläre Verabreichung von EDTA fuhrt zu Zellschäden und Schmerzen und ist daher kontraindiziert.
Autor: Dr. rer. nat. Joachim Exner